近日,基础医学院张茜副教授在《神经肿瘤学》(Neuro-Oncology)发表题为《NQO1介导胶质母细胞瘤氧化应激抵抗与肿瘤微环境重塑》(NQO1-mediated oxidative stress resistance and tumor microenvironment remodeling in glioblastoma)的研究论文。该研究发现了胶质母细胞瘤氧化应激抵抗与肿瘤微环境重塑的关键分子NAD(P)H:醌氧化还原酶1(NQO1),揭示了NQO1通过ROS-Lamin B1信号轴维持胶质瘤干细胞Lamin B1的稳定,进而抑制cGAS-STING通路和I型干扰素分泌,构建免疫抑制微环境。靶向NQO1及其下游效应分子如β-拉帕酮联合免疫检查点PD-1单抗,可同步瓦解氧化应激抵抗并重塑免疫微环境,为胶质瘤临床转化治疗提供了新思路。

胶质母细胞瘤(GBM)是颅内最致命的原发恶性肿瘤,手术联合放化疗仍难突破两年中位生存期,其高恶性源于复杂的肿瘤微环境。胶质瘤干细胞(GSCs)位于肿瘤微环境的顶端,是具有自我更新、多向分化和促使肿瘤形成的核心组分,为肿瘤复发和耐药埋下种子。此外,酸性、营养剥夺、缺氧和免疫浸润所引发的氧化应激,使活性氧(ROS)长期超载,驱动DNA损伤、脂质过氧化和代谢重 编程。GSCs如何借此强化抗氧化系统,与TME内免疫细胞相互作用以维持GSCs自身干性并实现免疫逃逸,机制仍待阐明。
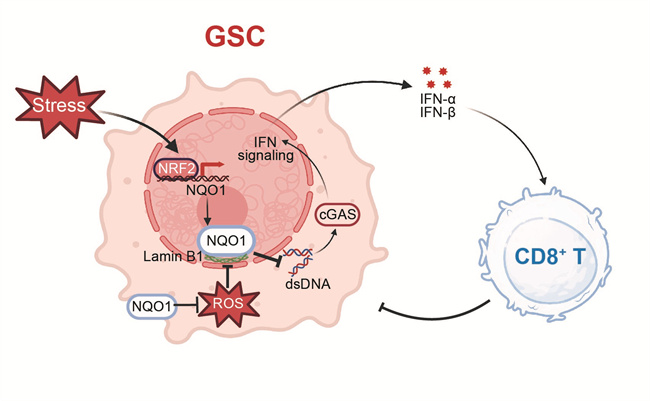
本研究通过整合蛋白组学与单细胞转录组数据发现,NQO1是维持GSCs抗氧化优势的核心分子。在应对过氧化氢和叔丁基过氧化氢诱导的氧化应激模型中,GSCs表现出高水平的抗氧化应激能力。NQO1通过维持ROS水平,不仅保护肿瘤细胞,更稳定核纤层蛋白Lamin B1,防止核膜破裂。一旦抑制 NQO1,dsDNA 大量泄漏至胞质,cGAS-STING 通路被强烈激活,I型干扰素分泌增加,肿瘤微环境内CD8+ T细胞浸润明显增多。机制上,NRF2转录上调 NQO1,进而抑制cGAS-STING信号,重塑免疫抑制微环境促使肿瘤细胞逃避免疫系统的监视和攻击。基于此,研究者采用NQO1底物β-拉帕酮联合PD-1单抗,可协同增强CD8+ T细胞浸润与杀伤效应,为胶质瘤免疫治疗提供新的临床转化依据。
基础医学院张茜副教授、生殖医学与子代健康全国重点实验室李朝军教授为本论文共同通讯作者。南京大学博士研究生李扬清、我校研究生康涛、贾臻、我校第一附属医院神经外科陆晨飞博士、我校研究生崔高源为本文的共同第一作者。此工作得到国家自然科学基金青年科学基金A类、国家自然科学基金面上项目、国家自然科学基金青年项目、肿瘤个体化协同创新中心临床研究基金项目、江苏省自然科学基金等项目资助。
原文链接:https://doi.org/10.1093/neuonc/noag015
(撰稿/张茜课题组;图片/张茜课题组;审核/陈峰 王觉进)

