近日,附属口腔医院傅瑜副教授、江宏兵教授团队在《自噬》(Autophagy)发表题为《线粒体自噬受损导致骨纤维异常增殖症成骨和矿化障碍》(Impaired mitophagy contributes to osteogenesis and mineralization disorders in fibrous dysplasia)的研究论文,本研究首次系统揭示了cAMP-PRKA通路通过调控线粒体动力学,进而控制线粒体自噬与ACP转运,最终影响骨矿化的作用机制。研究成果不仅深化了对骨形成过程中线粒体质量控制作用的认识,也为相关骨疾病及颅颌面骨发育异常的精准干预提供了新的理论基础和潜在治疗靶点。
骨纤维异常增殖症(fibrous dysplasia,FD)是一类由骨髓间充质干细胞GNAS基因激活突变引起的非遗传性骨疾病,以骨形成障碍与矿化缺陷为核心病理特征,其分子机制尚未完全阐明。既往研究提示,线粒体自噬在骨矿化前驱体无定型磷酸钙(ACP)的形成与转运过程中发挥关键作用,然而其在FD发生发展中的具体调控机制仍不清晰。
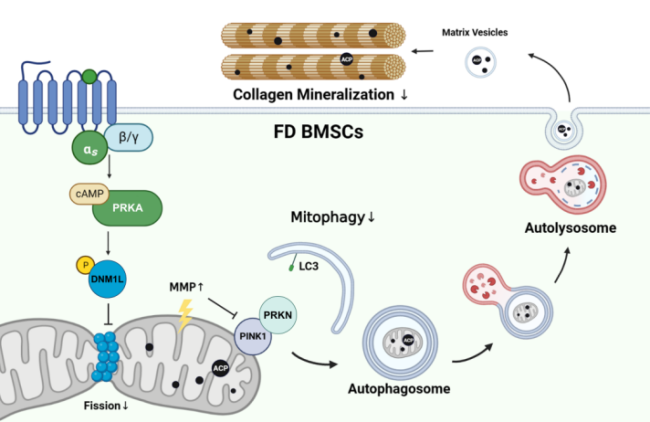
本研究围绕FD骨矿化障碍的核心科学问题展开,首次明确线粒体自噬受损是导致FD 成骨分化异常、骨矿化缺陷的关键原因。研究表明,在FD来源的骨髓间充质干细胞中,GNAS基因突变引发cAMP-PRKA信号通路持续激活,破坏线粒体稳态,抑制线粒体自噬,导致ACP生成与分泌显著减少,最终引发骨矿化障碍。
进一步机制研究发现,线粒体动力学失衡是线粒体自噬受损的核心基础。正常情况下,线粒体会在“分裂”和“融合”之间保持平衡。而在FD中,由于PRKA异常激活,会促进DNM1L/DRP1的特定位点(Ser637)发生磷酸化,使其难以进入线粒体,从而抑制分裂、增强融合。这种异常状态不仅抑制PINK1-PRKN依赖的线粒体自噬启动,也限制ACP在线粒体中的释放与转运,进一步加剧骨矿化障碍。
在干预策略研究层面,研究证实恢复线粒体分裂或特异性抑制PRKA活性可有效逆转上述异常过程。通过药物干预或基因手段调控促进DNM1L/DRP1功能,可恢复线粒体自噬水平,增强ACP分泌,并显著改善体外及三维骨微组织模型中的矿化能力。同时,相较于单纯激活线粒体自噬,调控线粒体分裂作为上游关键步骤,对矿化功能的恢复更为有效。
我校附属口腔医院口腔颌面外科傅瑜副教授、江宏兵教授为该论文共同通讯作者。我校附属口腔医院口腔颌面外科博士凌子吉为论文第一作者,该研究工作得到江苏省自然科学基金等项目的资助。
原文链接:https://doi.org/10.1080/15548627.2026.2643409
(供稿/附属口腔医院;审核/刘来奎)

