近日,基础医学院徐志鹏、季旻珺团队与中科院上海药物研究所周子凯团队合作在Cell Reports发表研究论文Maternal immune activation perturbs intestinal niche through microbial glycerophospholipids and drives offspring behavioral abnormalities。该研究通过弓形虫可溶性速殖子抗原(STAg)诱导的母体免疫激活(MIA)小鼠模型,系统揭示了孕期MIA通过肠道菌群代谢物(OMPC)介导子代孤独症谱系障碍(ASD)相关行为异常的分子机制,并提出鼠李糖乳杆菌(LGG)作为一种产前预防策略,可有效恢复肠道免疫稳态,缓解MIA引发的胎盘及胎儿神经炎症,并挽救子代行为缺陷。
孤独症谱系障碍(ASD)是一种由遗传与环境多因素交互作用所致的慢性神经发育障碍性疾病(NDDs),广泛累及认知、运动、社会适应及行为等多个维度,严重阻碍患儿的生长发育与身心健康。母体免疫激活(MIA)已被确认为母体感染诱发子代ASD发生的关键驱动因素。因此,深入解析孕期母体免疫状态调控子代孤独症发生的分子网络,并探寻有效的早期干预靶点与策略,对于促进儿童精神健康及实现重大神经发育障碍的源头防控具有重要的临床意义。
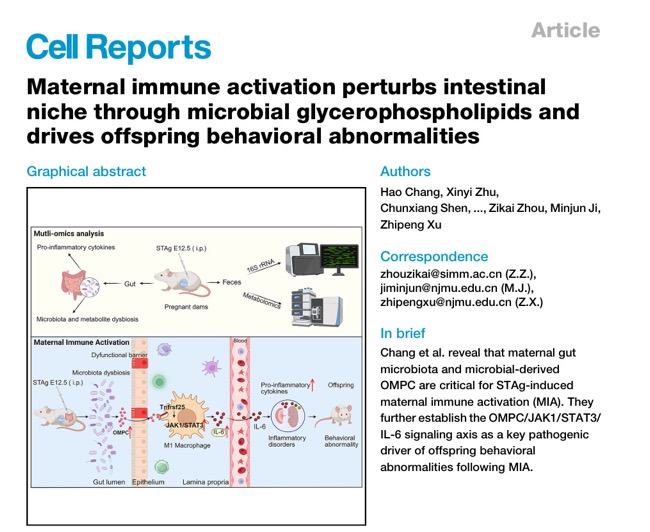
基于本团队前期建立的弓形虫可溶性速殖子抗原(STAg)诱导的MIA小鼠模型(Nature Neuroscience, 2021),进一步解析了STAg-MIA孕鼠肠道、胎盘及胎脑的病理学演变。发现MIA孕鼠肠道促炎应答显著增强,以M1型巨噬细胞极化及关键促炎细胞因子IL-6的显著上调为核心特征。通过整合肠道菌群与代谢物谱分析,揭示弓形虫MIA孕鼠存在肠道菌群失衡及代谢谱显著紊乱,其中促炎型代谢物1-oleoyl-2-myristoyl-sn-glycero-3-phosphocholine(OMPC)显著升高,进而导致胎盘和胎脑促炎表型显著上调,并诱发子代行为学异常。研究还证实母体IL-6信号通路在弓形虫诱导MIA致子代行为异常中发挥关键介导作用。本研究首次阐明:OMPC通过结合巨噬细胞表面的Tnfrsf25受体,激活JAK1/STAT3/IL-6炎性信号轴,致使孕鼠肠道及外周血IL-6水平显著升高,最终导致子代行为学异常。
鉴于STAg-MIA孕鼠肠道炎症增加,研究团队在孕早期给予鼠李糖乳杆菌LGG(一种抗炎的益生菌)口服补充干预可有效抑制母体肠道IL-6表达,修复肠道屏障损伤,并显著减轻STAg-MIA孕鼠胎盘和胎脑的炎症反应,能预防子代行为学异常的发生。这一发现为MIA相关神经发育障碍的早期干预提供潜在可行的临床前(Pre-Clinical)转化方向。
本研究揭示了以弓形虫抗原为诱因的母体免疫激活(MIA)模型中的完整致病链条。不仅为MIA导致子代NDDs的发病机制提供新的理论框架,也突破了MIA研究领域长期以来对上游驱动因素认识的局限。同时,该研究提出并验证了益生菌LGG作为产前预防策略的有效性,为ASD及其他NDDs的早期干预提出新思路。
我校博士生常浩为第一作者。我校徐志鹏、季旻珺以及中科院上海药物研究所周子凯为共同通讯作者。该项目得到国家自然科学基金面上项目、江苏省自然科学杰出青年基金等项目资助。
原文链接:https://www.cell.com/cell-reports/fulltext/S2211-1247(26)00289-5
(供稿/徐志鹏 季旻珺 周子凯研究团队;审核/王觉进)

